¶ 지식 정보
¶ 성질
물질을 설명하거나 확인하는 데 이용되는 특성이다.
¶ 물리적 성질과 화학적 성질
물질의 고유한 변화를 포함하지 않는 성질을 물리적 성질, 포함하는 성질을 화학적 성질이라 한다.
¶ 물리적 성질과 화학적 성질 예시
- 물리적 성질 예시:
종이를 접을 때 종이의 모양 변화 (물질의 고유한 성질은 달라지지 않음) - 화학적 성질 예시:
종이를 태우면 종이의 고유한 성질 변화 (태운 이후엔 더 이상 불에 타지 않음)
¶ 금속 원소, 비금속 원소, 준금속 원소
¶ 금속 원소
열과 전류(전하의 흐름)가 매우 잘 흐르고, 광택이 있으며, 상온()에서 액체 상태인 수은을 제외하면 고체 상태로 존재하는 원소이다.
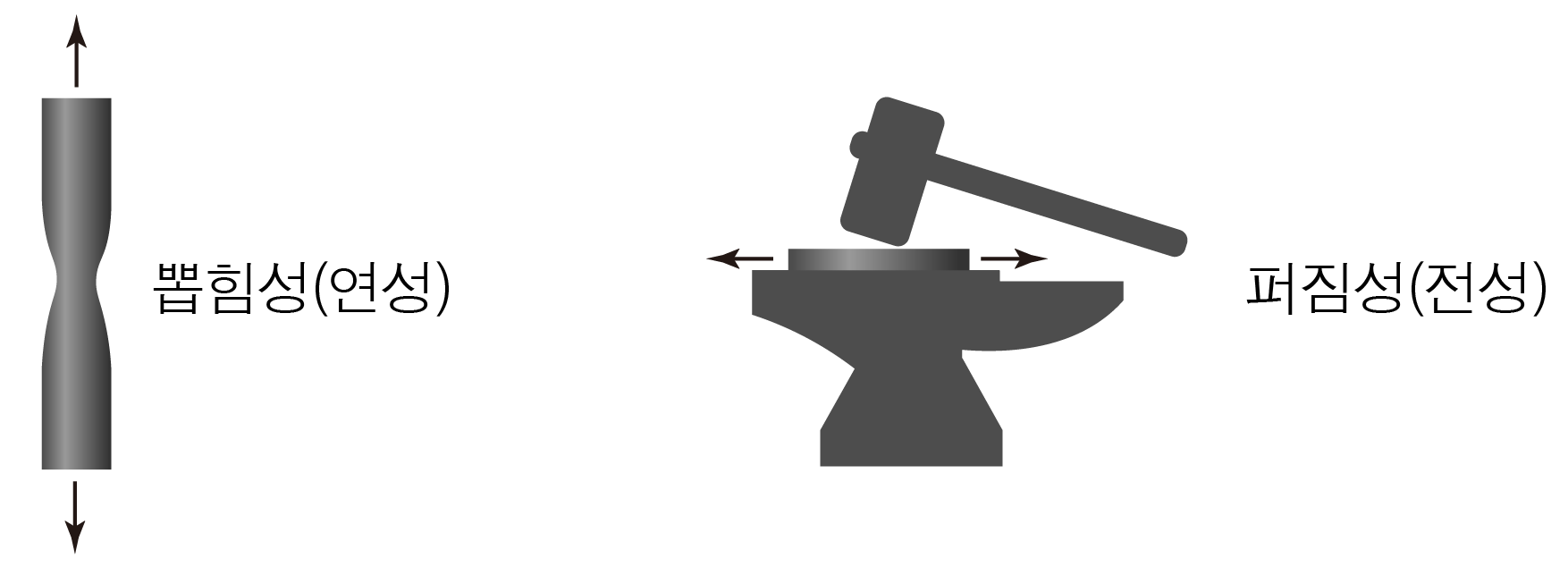
힘을 가해도 쉽게 부서지지 않고 길게 늘어나는 성질인 뽑힘성(연성)과 퍼지는 성질인 펴짐성(전성)이 나타난다.
¶ 비금속 원소
열과 전류가 거의 흐르지 못하고, 상온()에서 액체 상태인 브로민을 제외하면 대부분 기체나 고체 상태로 존재하는 원소이다.
¶ 준금속 원소
¶ 보어의 원자 모형
원자의 중심에 원자핵이 있고, 전자가 전자 껍질을 따라 원자핵 주위를 도는 모형이다.
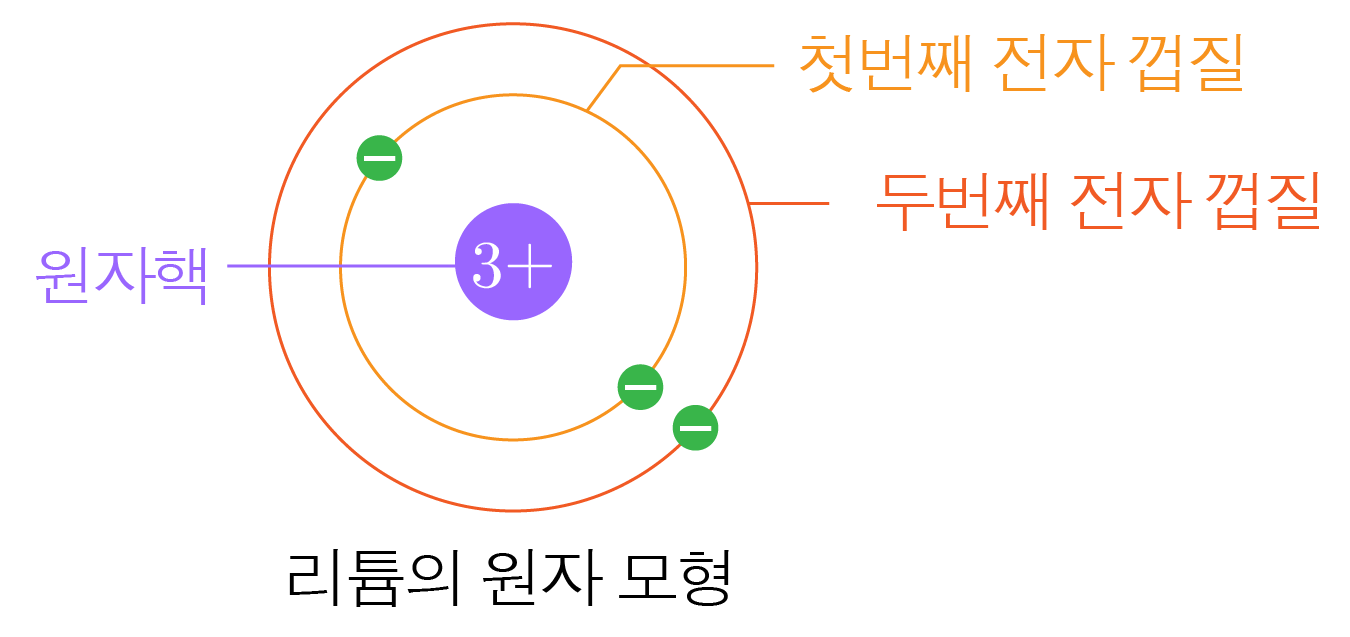
편의를 위해 양성자와 중성자로 구성된 원자핵은 상대적 전하와 함께 하나로 나타내었다.
¶ 전자 껍질
특정 에너지 값을 갖는 궤도이다.
보어의 원자 모형에서는 전자가 도는 궤도에 해당한다.
¶ 주기율표
원자 번호와 화학적 성질에 따라 원소를 배열한 표이다.
원소 기호 위는 원자 번호, 아래는 원소의 이름을 나타낸다.
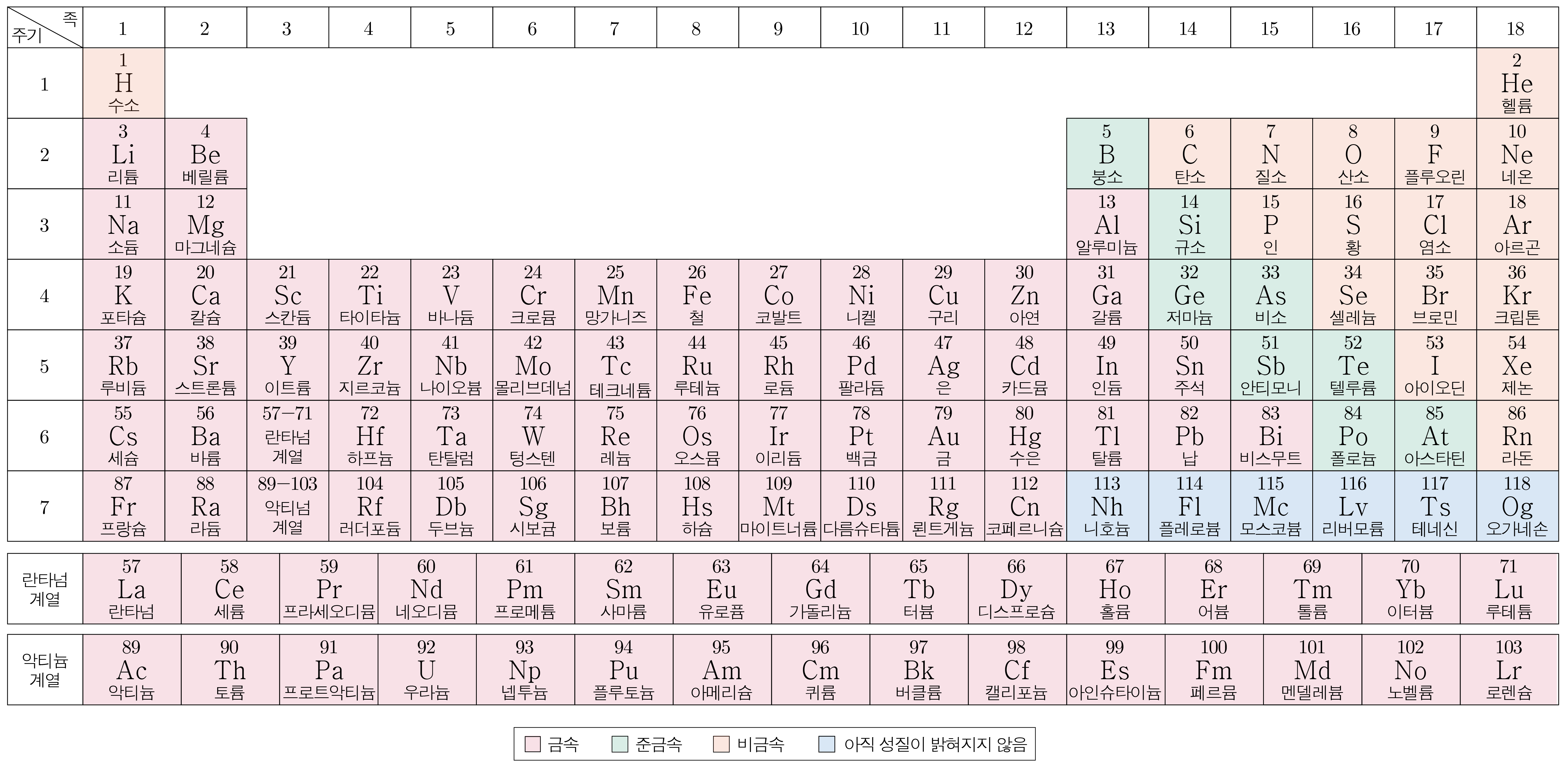
원자 번호 번부터 번까지 매우 자주 쓰이므로 원소 기호와 이름을 암기해야 하며,
원자 번호 번인 수소는 족임에도 금속이 아닌 비금속임에 주의한다.
란타넘 계열과 악티늄 계열 관련 설명은 추후 진행한다.
¶ 주기와 족
주기율표에서 가로줄을 주기, 세로줄을 족이라 한다.
같은 족 원소는 원자가전자 수가 같아 화학적 성질이 유사하며, 같은 주기 원소는 전자 껍질 수가 같다.
¶ 전자 껍질에 전자가 채워지는 방식
원자 번호가 커짐에 따라 원자핵에서 가까운 전자 껍질부터 전자가 차례대로 채워지며,
주기 원소에서 첫 번째 전자 껍질에는 최대 개의 전자가,
두 번째와 세 번째 전자 껍질에는 각각 최대 개의 전자가 채워질 수 있다.
¶ 전자 껍질에 전자가 채워지는 방식 예시
주기에 해당하는 원자 번호가 번(수소)부터 번(헬륨)까지는 첫 번째 전자 껍질에 전자가 채워지고,
주기에 해당하는 번(리튬)부터 번(네온)까지는 두 번째 전자 껍질에 전자가 채워지며,
주기에 해당하는 번(소듐)부터 번(아르곤)까지는 세 번째 전자 껍질에 전자가 채워진다.
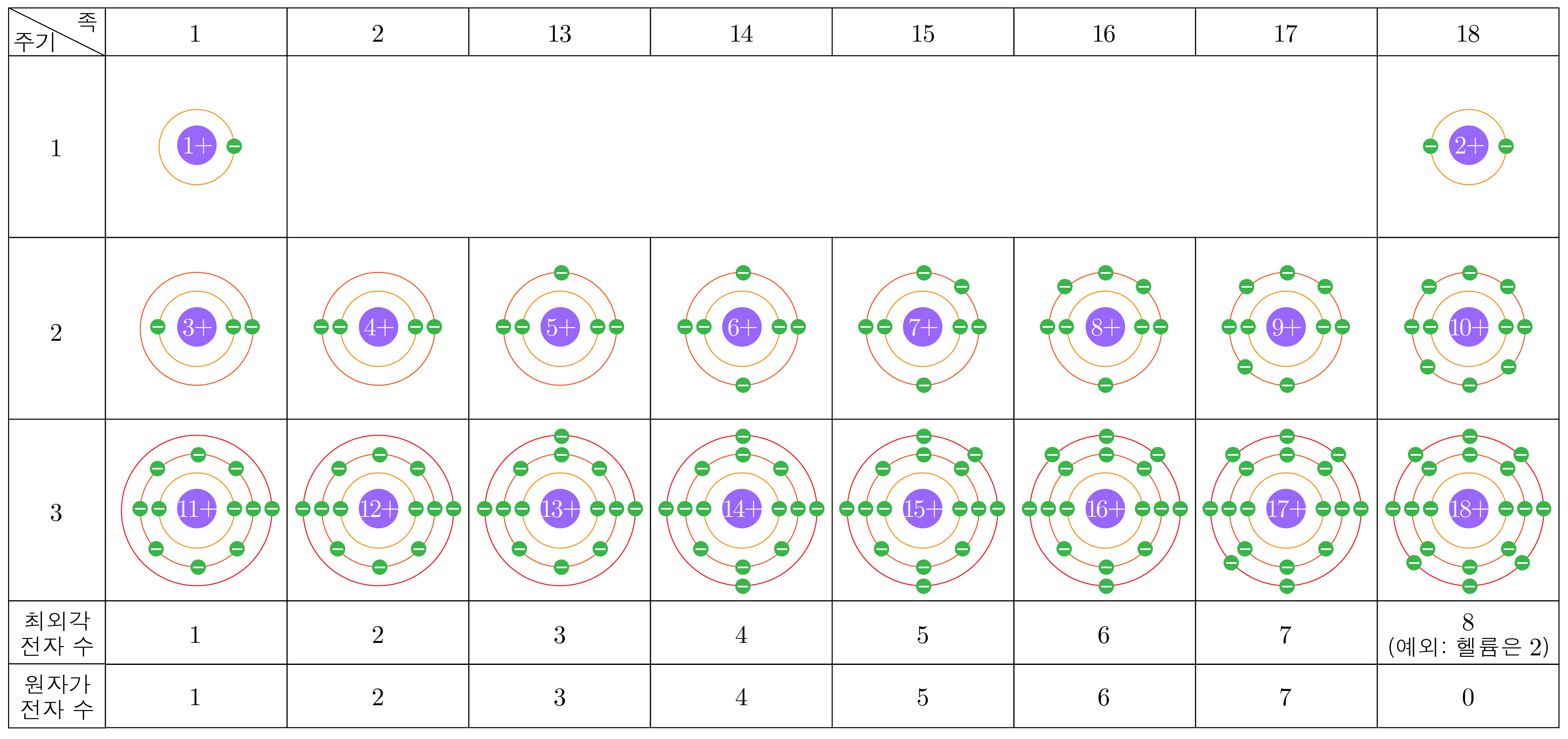
¶ 최외각전자와 원자가전자
가장 바깥 전자 껍질에 있는 전자는 최외각전자라 하며,
이 중 화학 반응에 참여할 수 있는 전자를 원자가전자라 한다.
¶ 옥텟 규칙과 듀엣 규칙
옥텟 규칙은 가장 바깥 전자 껍질에 전자 개를 채워 안정해지려는 경향을 말한다.
옥텟 규칙의 예외로 주기인 수소와 헬륨은 전자 껍질에 전자 개만 채워도 안정해지며, 이를 듀엣 규칙이라고도 한다.
¶ 족에 따른 원소의 특징
주기율표 상에서 왼쪽에 있는 원소는 전자를 잃어서, 오른쪽에 있는 원소는 전자를 얻어서 옥텟 규칙을 만족하려 한다.
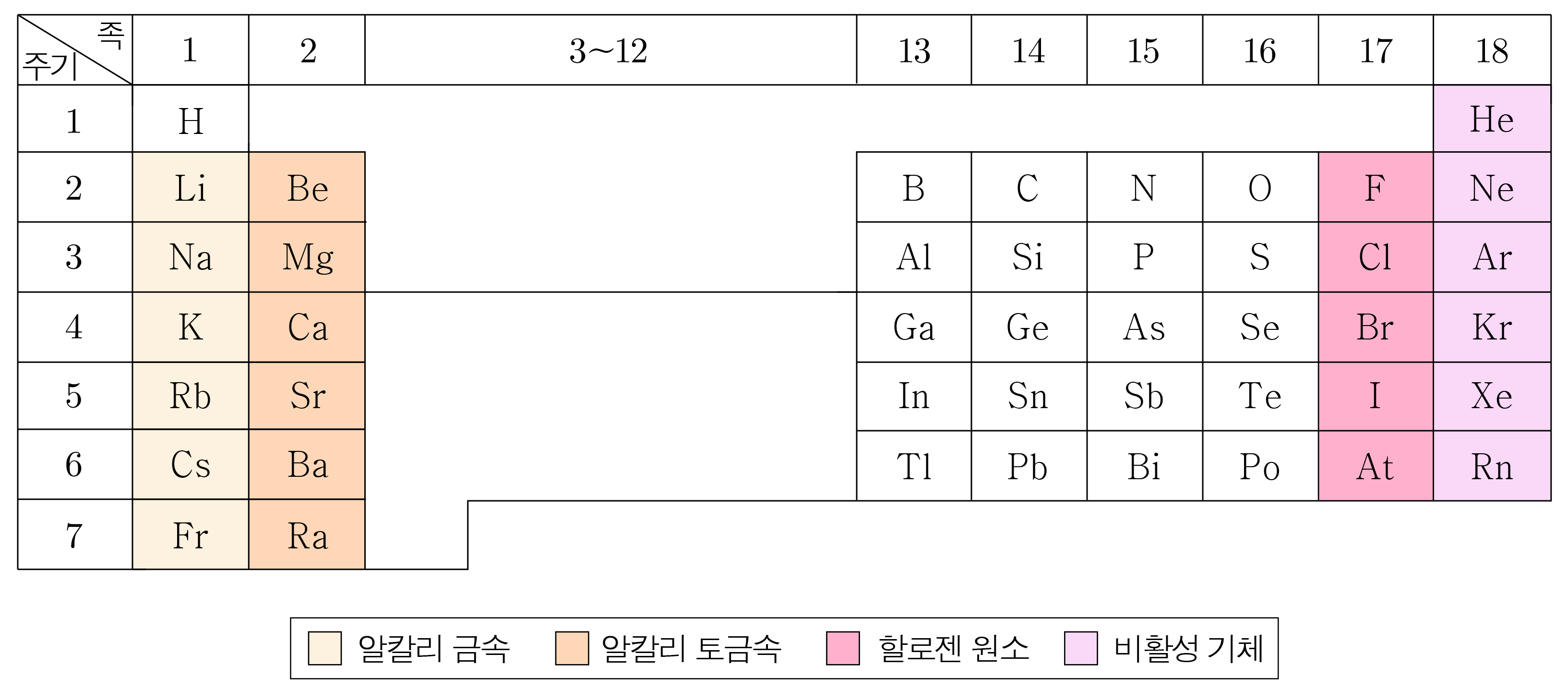
-
족 원소와 족 원소:
족 원소는 알칼리 금속으로 전자 개를 잃어 양이온이 되려는 성질이 있으며,
족 원소는 알칼리 토금속으로 전자 개를 잃어 양이온이 되려는 성질이 있다.
족 원소와 족 원소 모두 순수한 상태에선 광택을 띠지만 반응성이 매우 커 상온에 두면 산소와 반응하여 광택을 잃는다.
-
족 원소:
할로젠이라고도 하며, 전자 개를 얻어 음이온이 되려는 성질이 있고, 반응성이 매우 커 금속이나 수소와 잘 반응한다.
-
족 원소:
대부분의 원소는 최외각전자의 수와 원자가전자의 수가 같다.
그러나 족 원소는 최외각전자의 개수가 개로 옥텟 규칙을 만족하면서, 원자가전자의 개수가 개이므로 화학적으로 매우 안정하다.
따라서 다른 물질과 거의 반응하지 않아 비활성 기체라고 한다.
¶ 여러가지 이름으로 불리는 원소
표기 방식 - 원래 이름(원소 기호, 원자 번호): 다른 이름
- 플루오린(, ): 불소
- 소듐(, ): 나트륨
- 규소(, ): 실리콘
- 포타슘(, ): 칼륨
- 아이오딘(, ): 요오드
¶ 적용 문항
¶ 1번 문항

¶ 2번 문항




