¶ 지식 정보
¶ 화학 결합
두 개 이상의 원자가 하나의 집합체를 만들 수 있도록 해주는 결합이다.
화학 결합의 종류로는 공유 결합, 이온 결합, 금속 결합 등이 있다.
¶ 공유 결합
서로 전자를 공유하여 전자쌍을 형성하는 결합이며, 주로 비금속과 비금속 원소 사이에 형성된다.
공유 결합을 통해 각 원자는 듀엣 규칙(수소나 헬륨) 또는 옥텟 규칙(그 외 원소)을 만족하여 더 안정해질 수 있다.
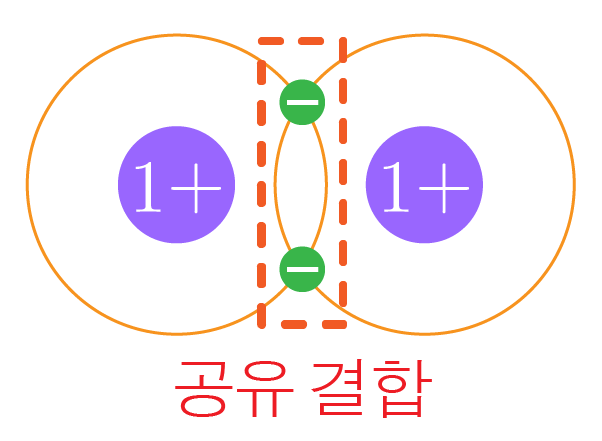
두 개의 수소 원자는 공유 결합을 통해 전자를 공유하여 더 안정한 상태인 $\mathrm{H_2}$를 형성한다.
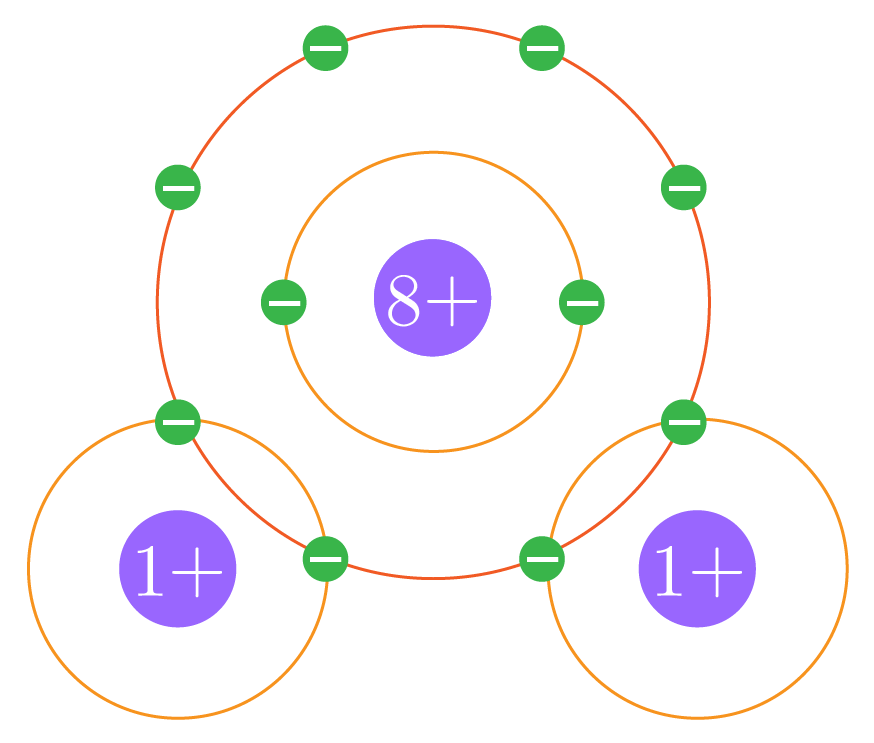
¶ 공유 결합 예시
그림과 같이 한 개의 산소 원자는 두 개의 수소 원자와 공유 결합을 통해 더 안정한 상태인 를 형성한다.
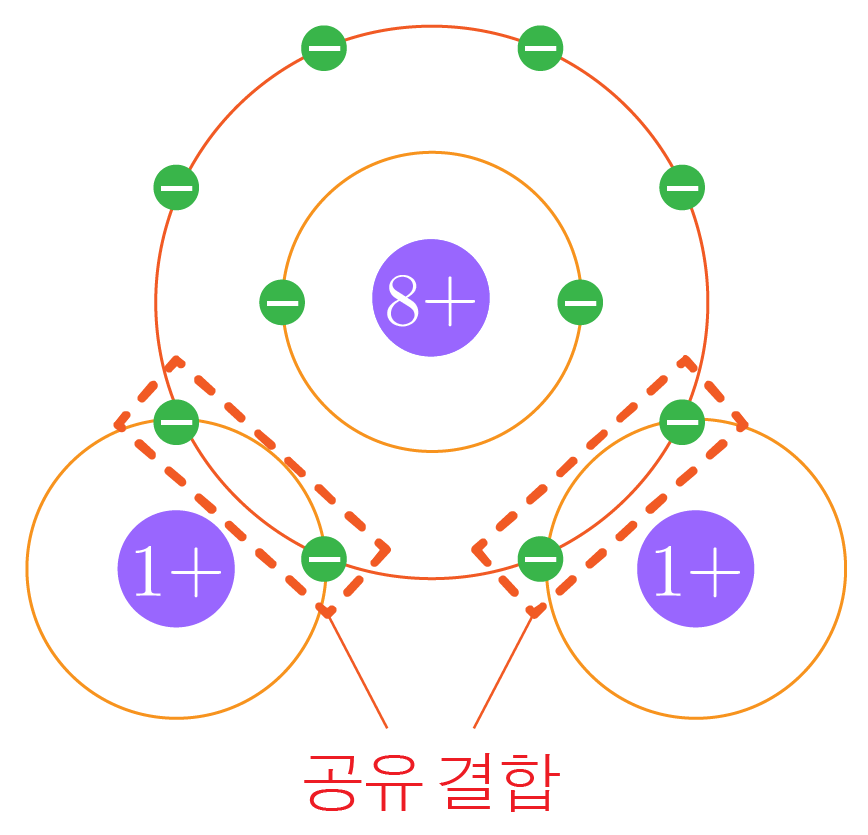
¶ 분자
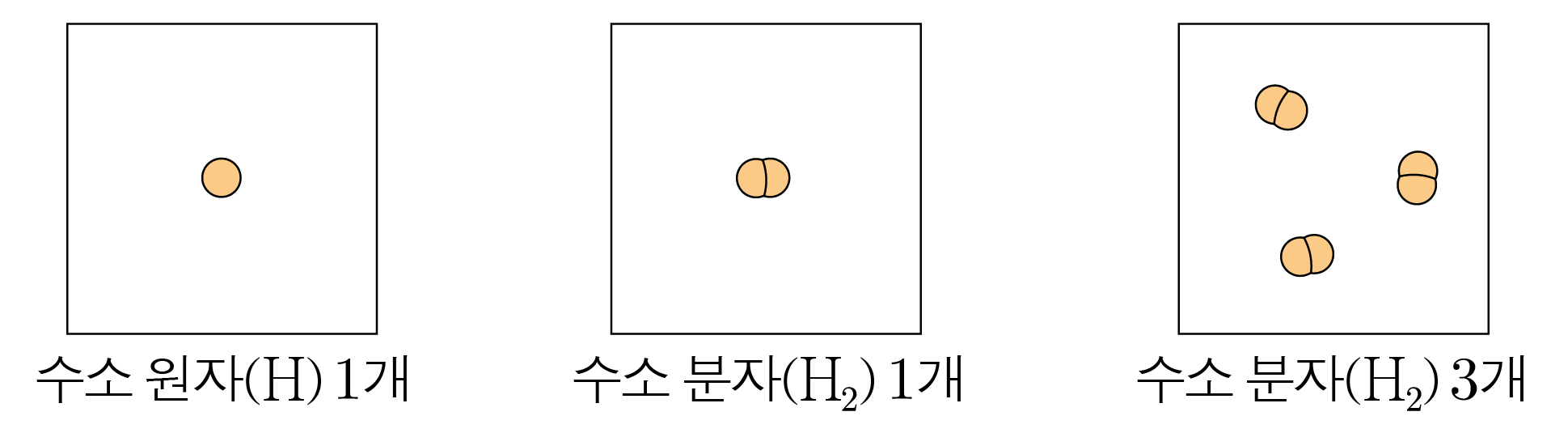
두 개 이상의 원자가 공유 결합하여 독립적으로 존재할 수 있는 물질 단위이다.
¶ 단원자 분자(일원자 분자)
비활성 기체(헬륨(), 네온(), 아르곤() 등)와 같이 원자 하나로도 분자의 특징을 가지는 원자이다.
¶ 분자의 표기
- 원자 수 표기:
원소 기호의 오른쪽 아래에 표기하고, 원자 수가 개인 경우 생략한다. - 분자의 개수 표기:
분자의 구성 원자를 나타내는 분자식 앞에 숫자로 표기하고, 개인 경우 생략한다.
¶ 분자의 표기 예시
수소 원자 개가 결합하여 이루어진 수소 분자는 로 표기한다.
두 개의 수소 원자와 한 개의 산소 원자가 결합하여 이루어진 물 분자는 로 표기하며,
세 개의 물 분자를 나타낼 경우 로 표기한다.
¶ 이온 결합
양이온과 음이온 사이의 서로 끌어당기는 힘(인력)에 의해 형성되는 결합이다.
주로 금속과 비금속 원소 사이에 형성된다.
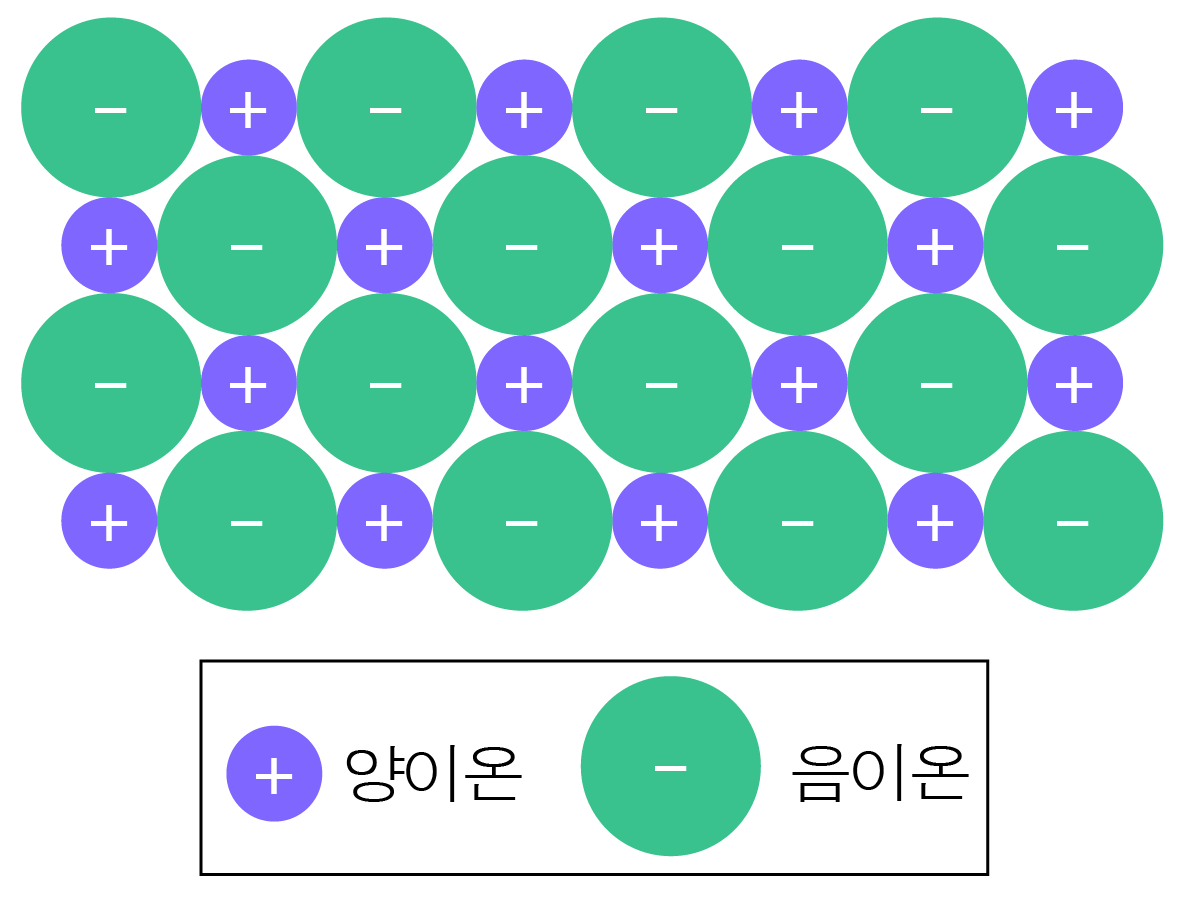
¶ 이온 결합 물질의 표기
이온 결합은 수많은 이온이 연속적으로 결합하고 있어 이온 결합 물질의 화학식을 나타낼 때는 실제 원자 수로 나타내지 않고,
양이온과 음이온의 균형을 맞춰 전기적으로 중성인 가장 간단한 정수비로 나타낸다.
¶ 이온 결합 물질의 표기 예시
- 와 가 결합하여 만든 염화나트륨은 와 이 의 비율을 이루어야 전기적으로 중성이 되므로
화학식은 과 같이 표기한다. - 와 가 결합하여 만든 염화칼슘은 과 이 의 비율을 이루어야 전기적으로 중성이 되므로
화학식은 와 같이 표기한다.
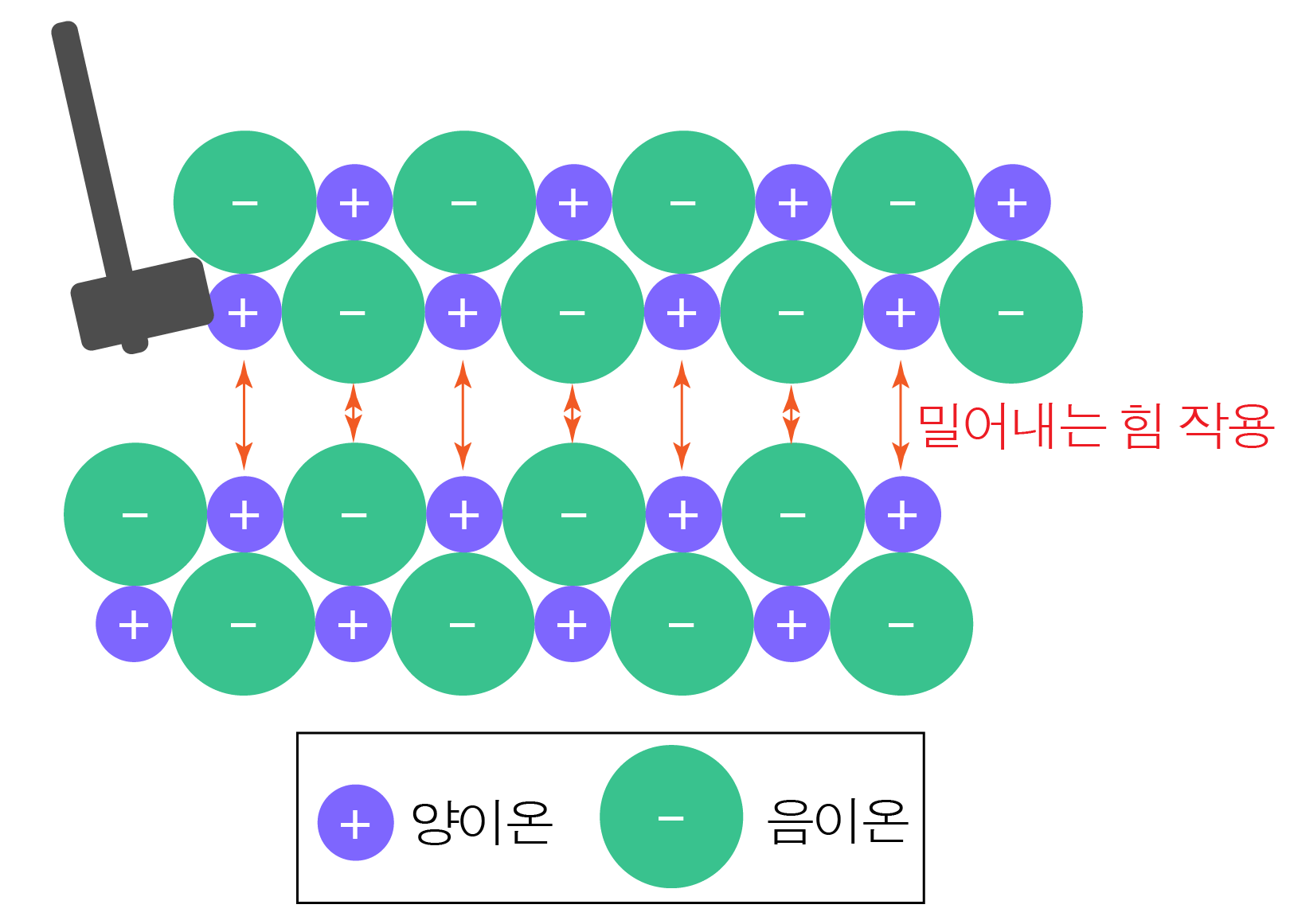
¶ 이온 결합 물질의 특징
힘을 가하게 되면 층이 밀리면서 같은 전하를 띤 이온이 가까워져 서로를 밀어내므로 쉽게 부서진다.
¶ 금속 결합
금속 양이온과 자유 전자 사이의 서로 끌어당기는 힘(인력)에 의해 형성되는 결합이다.
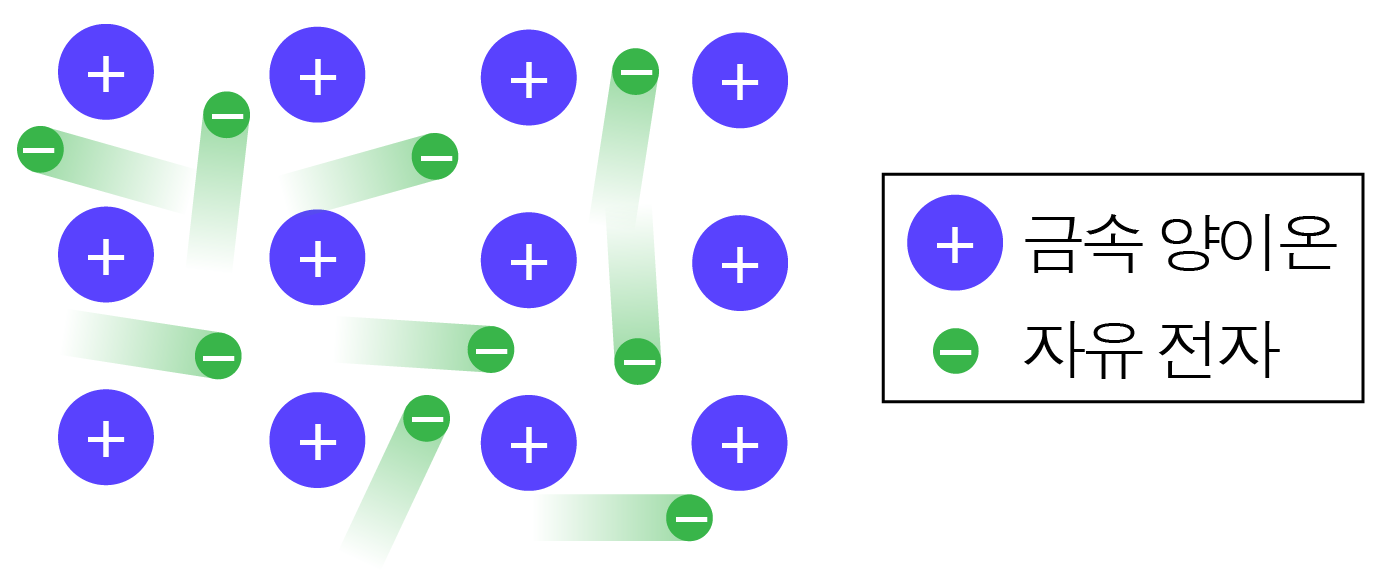
¶ 자유 전자
금속 원자가 내놓은 전자로, 금속 양이온 사이를 자유롭게 움직이면서 금속 양이온과 결합하는 전자이다.
이 자유 전자로 인해 힘을 가해도 쉽게 부서지지 않고 길게 늘어나는 성질인 뽑힘성(연성)과 퍼지는 성질인 펴짐성(전성)이 나타난다.
¶ 금속 결합 물질의 표기
금속 원소 하나로 이루어진 경우 원소 기호만을 사용하여 표기한다.
¶ 금속 결합 물질의 표기 예시
철로만 이루어진 물질은 로, 구리로만 이루어진 물질은 로 표기한다.
¶ 전기 전도성
전기(전류)가 흐르는 성질이다. 전기를 전도할 수 있으면(전류가 흐를 수 있으면) 전기 전도성을 가진다.
¶ 결합의 종류와 물체의 상태에 따른 전기 전도성
공유 결합 물질은 전자가 공유 결합으로 묶여 있어 자유롭게 이동할 수 없다.
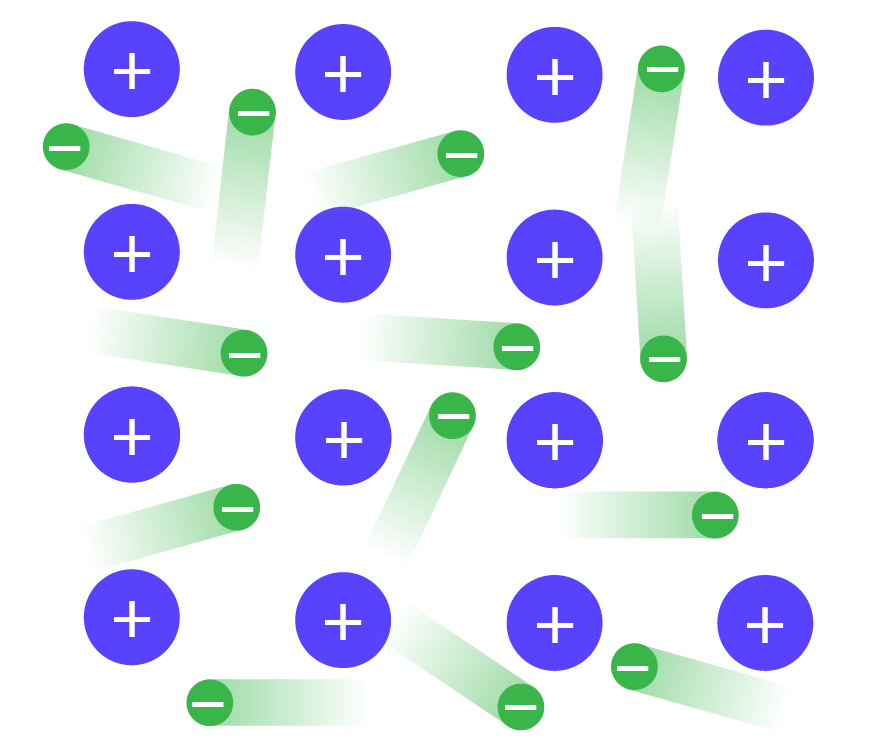
금속 결합 물질은 자유롭게 이동할 수 있는 자유 전자를 가진다.

고체 상태의 이온 결합 물질에서는 이온이 자유롭게 이동할 수 없다.
액체나 수용액 상태의 이온 결합 물질에서는 이온이 자유롭게 이동할 수 있다.
¶ 적용 문항
¶ 1번 문항

¶ 2번 문항




