| 해당 지식 |

|
| 하위 지식 |
상위 지식 |

|
$-$
|
어떤 물질 1mol의 상태가 변할 때의 반응 엔탈피이다.
상변화 엔탈피의 종류에는 승화 엔탈피, 응축(액화) 엔탈피, 기화 엔탈피, 융해 엔탈피, 응고 엔탈피가 있다.
다음은 25∘C에서 H2O의 열화학 반응식에 대한 자료이다.
H2O의 표준 융해 엔탈피와 표준 응고 엔탈피를 구해보자.
H2O(s)→H2O(l)ΔH∘=6kJ
고체 상태의 H2O 1mol이 액체 상태로 변할 때의 표준 반응 엔탈피(ΔH∘)는 6kJ이므로
H2O의 표준 융해 엔탈피는 6kJ/mol이다.
또한 역반응은 아래와 같으므로 H2O의 표준 응고 엔탈피는 −6kJ/mol이다.
H2O(l)→H2O(s)ΔH∘=−6kJ
고체 상태의 이온 결합 물질 1mol을 기체 상태의 양이온과 음이온으로 만들 때 흡수되는 에너지이다.
단위는 주로 kJ/mol을 사용한다.
격자 에너지는 흡수되는 에너지(흡열 반응, ΔH>0)에 해당하므로
기체 상태의 양이온과 음이온으로부터 고체 상태의 이온 결합 물질 1mol이 형성되는 반응의 반응 엔탈피는
격자 에너지와 크기가 같고 부호가 반대이다.
다음은 25∘C에서 Na+(g)와 F−(g)의 반응의 열화학 반응식이다.
표준 상태에서 NaF(s)의 격자 에너지는?
Na+(g)+F−(g)→NaF(s)ΔH∘=−923kJ
표준 상태에서 기체 상태의 양이온인 Na+(g)와 음이온인 F−(g)가 반응하여 고체 상태의 NaF(s) 1mol이 생성될 때,
923kJ만큼 에너지가 방출되므로 표준 상태에서 NaF(s)의 격자 에너지는 923kJ/mol이다.
고체와 기체 상태의 반응물이 반응하여 이온 결합 물질을 생성하는 반응은 반응 엔탈피(ΔH)를 직접 측정하기 매우 힘드므로, 반응을 여러 단계로 나누어 헤스의 법칙을 활용하여 구하는 것이다.
보른-하버 순환은 아래와 같은 과정을 거친다.
1. 반응물의 공유 결합을 모두 끊고 기체 상태의 중성 원자로 만든다. (결합 해리 에너지, 상변화 에너지 활용)
2. 생성물에서 양이온을 이루는 원소의 중성 원자를 양이온으로 이온화시킨다. (이온화 에너지 활용)
3. 생성물에서 음이온을 이루는 원소의 중성 원자를 음이온으로 이온화시킨다. (전자 친화도 활용)
4. 양이온과 음이온을 결합시켜 이온 결합 물질을 만든다. (격자 에너지 활용)
다음은 25∘C에서 Na(s)와 Cl2(g)의 반응의 열화학 반응식과 표준 상태에서 반응식과 관련된 자료이다. 자료로부터 구한 x는?
2Na(s)+Cl2(g)→2NaCl(s)ΔH∘=xkJ
$\circ$ $\mathrm{Na}(s)$의 승화 엔탈피: $109\,\mathrm{kJ/mol}$
$\circ$ $\mathrm{Na}(g)$의 제 $1$ 이온화 에너지: $496\,\mathrm{kJ/mol}$
$\circ$ $\mathrm{Cl_2}(g)$의 결합 해리 에너지: $243\,\mathrm{kJ/mol}$
$\circ$ $\mathrm{Cl}(g)$의 전자 친화도: $-349\,\mathrm{kJ/mol}$
$\circ$ $\mathrm{NaCl}(s)$의 격자 에너지: $787\,\mathrm{kJ/mol}$
|
1. 반응물의 공유 결합을 모두 끊고 기체 상태의 중성 원자로 만든다. (결합 해리 에너지, 상변화 에너지 활용)
- Cl2(g)의 결합 해리 에너지가 243kJ/mol이므로
Cl2(g) 1mol에서 Cl 원자 사이의 공유 결합을 모두 끊어 Cl(g) 2mol을 만들 때 흡수되는 에너지는
243kJ이다.
- Na(s)의 승화 엔탈피가 109kJ/mol이므로
Na(s) 2mol을 Na(g) 2mol로 만들 때 흡수되는 에너지는
109kJ/mol×2mol=218kJ이다.
2. 생성물에서 양이온을 이루는 원소의 중성 원자를 양이온으로 이온화시킨다. (이온화 에너지 활용)
생성물인 NaCl(s)에서 양이온은 Na+에 해당하므로 양이온을 이루는 원소인 Na를 양이온으로 이온화시킨다.
Na(g)의 제1 이온화 에너지는 496kJ/mol이므로
Na(g) 2mol에서 전자 2mol을 떼어 Na+(g) 2mol을 만들 때 흡수되는 에너지는
496kJ/mol×2mol=992kJ이다.
3. 생성물에서 음이온을 이루는 원소의 중성 원자를 음이온으로 이온화시킨다. (전자 친화도 활용)
생성물인 NaCl(s)에서 음이온은 Cl−에 해당하므로 음이온을 이루는 원소인 Cl을 음이온으로 이온화시킨다.
Cl(g)의 전자 친화도는 −349kJ/mol이므로
Cl(g) 2mol에서 전자 2mol을 추가하여 Cl−(g) 2mol을 만드는 데 방출되는 에너지는
349kJ/mol×2mol=698kJ이다.
4. 양이온과 음이온을 결합시켜 이온 결합 물질을 만든다. (격자 에너지 활용)
NaCl(s)의 격자 에너지는 787kJ/mol이므로
Na+(g) 2mol과 Cl−(g) 2mol이 반응하여 NaCl(s) 2mol을 만들 때 방출되는 에너지는
787kJ/mol×2mol=1574kJ이다.
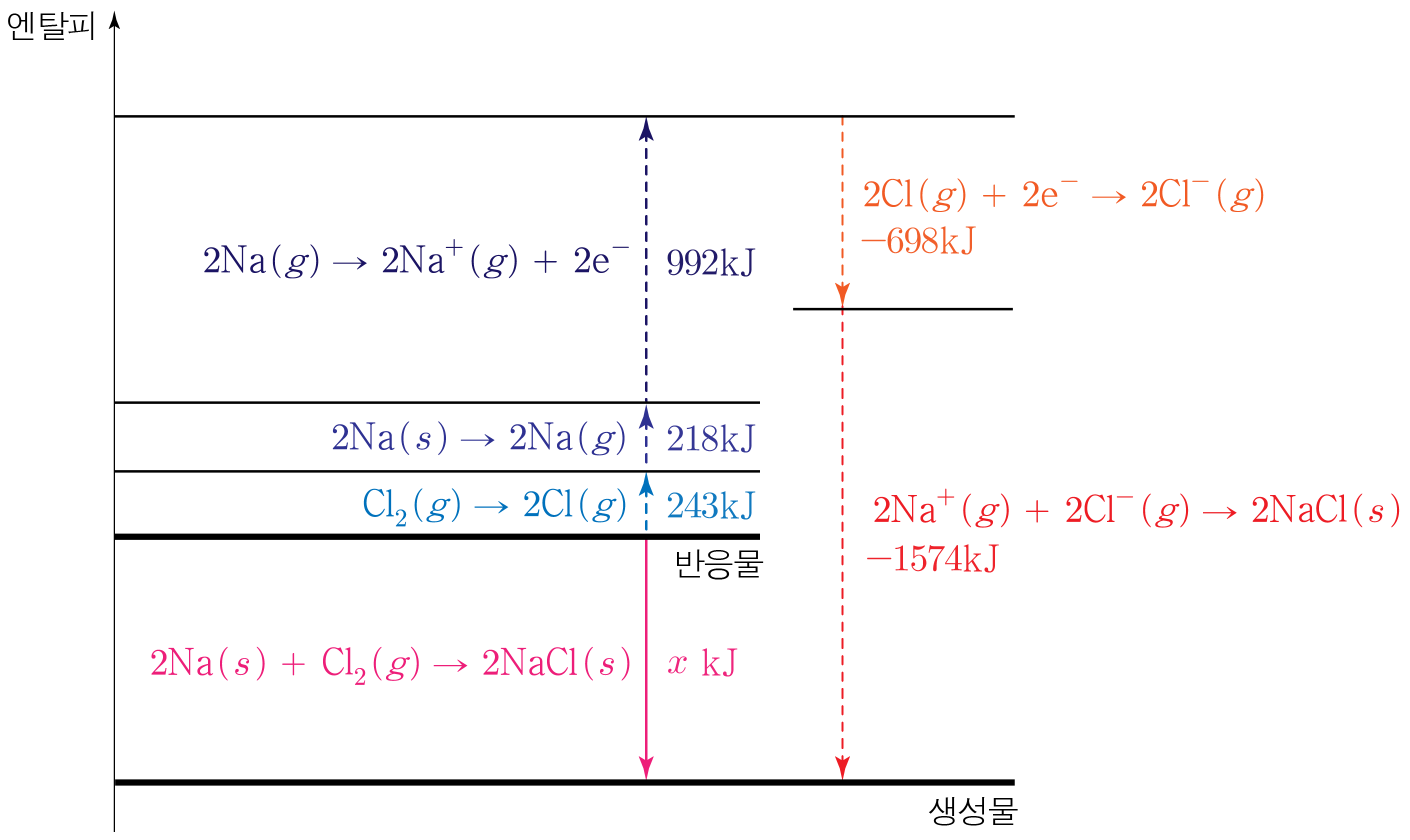
따라서 엔탈피 변화 과정을 나타내면 아래 그림과 같다.
그러므로
218kJ+243kJ+992kJ−698kJ−1574kJ=xkJ,
461kJ+992kJ−698kJ−1574kJ=xkJ,
1453kJ−698kJ−1574kJ=xkJ,
755kJ−1574kJ=xkJ,
−819kJ=xkJ,
x=−819이다.

정답: $3$
1. 반응물의 공유 결합을 모두 끊고 기체 상태의 중성 원자로 만든다. (결합 해리 에너지, 상변화 에너지 활용)
- F2(g)의 결합 해리 에너지가 159kJ/mol이므로
F2(g) 1mol에서 F 원자 사이의 공유 결합을 모두 끊어 F(g) 2mol을 만들 때 흡수되는 에너지는
159kJ이다.
- K(s)의 승화 엔탈피가 89kJ/mol이므로
K(s) 2mol을 K(g) 2mol로 만들 때 흡수되는 에너지는
89kJ/mol×2mol=178kJ이다.
2. 생성물에서 양이온을 이루는 원소의 중성 원자를 양이온으로 이온화시킨다. (이온화 에너지 활용)
생성물인 KF(s)에서 양이온은 K+에 해당하므로 양이온을 이루는 원소인 K를 양이온으로 이온화시킨다.
K(g)의 제1 이온화 에너지는 419kJ/mol이므로 K(g) 2mol에서 전자 2mol을 떼어 K+(g) 2mol을 만들 때 흡수되는 에너지는 419kJ/mol×2mol=838kJ이다.
3. 생성물에서 음이온을 이루는 원소의 중성 원자를 음이온으로 이온화시킨다. (전자 친화도 활용)
생성물인 KF(s)에서 음이온은 F−에 해당하므로 음이온을 이루는 원소인 F를 음이온으로 이온화시킨다.
F(g)의 전자 친화도는 −328kJ/mol이므로
F(g) 2mol에서 전자 2mol을 추가하여 F−(g) 2mol을 만드는 데 방출되는 에너지는
328kJ/mol×2mol=656kJ이다.
4. 양이온과 음이온을 결합시켜 이온 결합 물질을 만든다. (격자 에너지 활용)
KF(s)의 격자 에너지는 820kJ/mol이므로
K+(g) 2mol과 F−(g) 2mol이 반응하여 KF(s) 2mol을 만들 때 방출되는 에너지는
820kJ/mol×2mol=1640kJ이다.
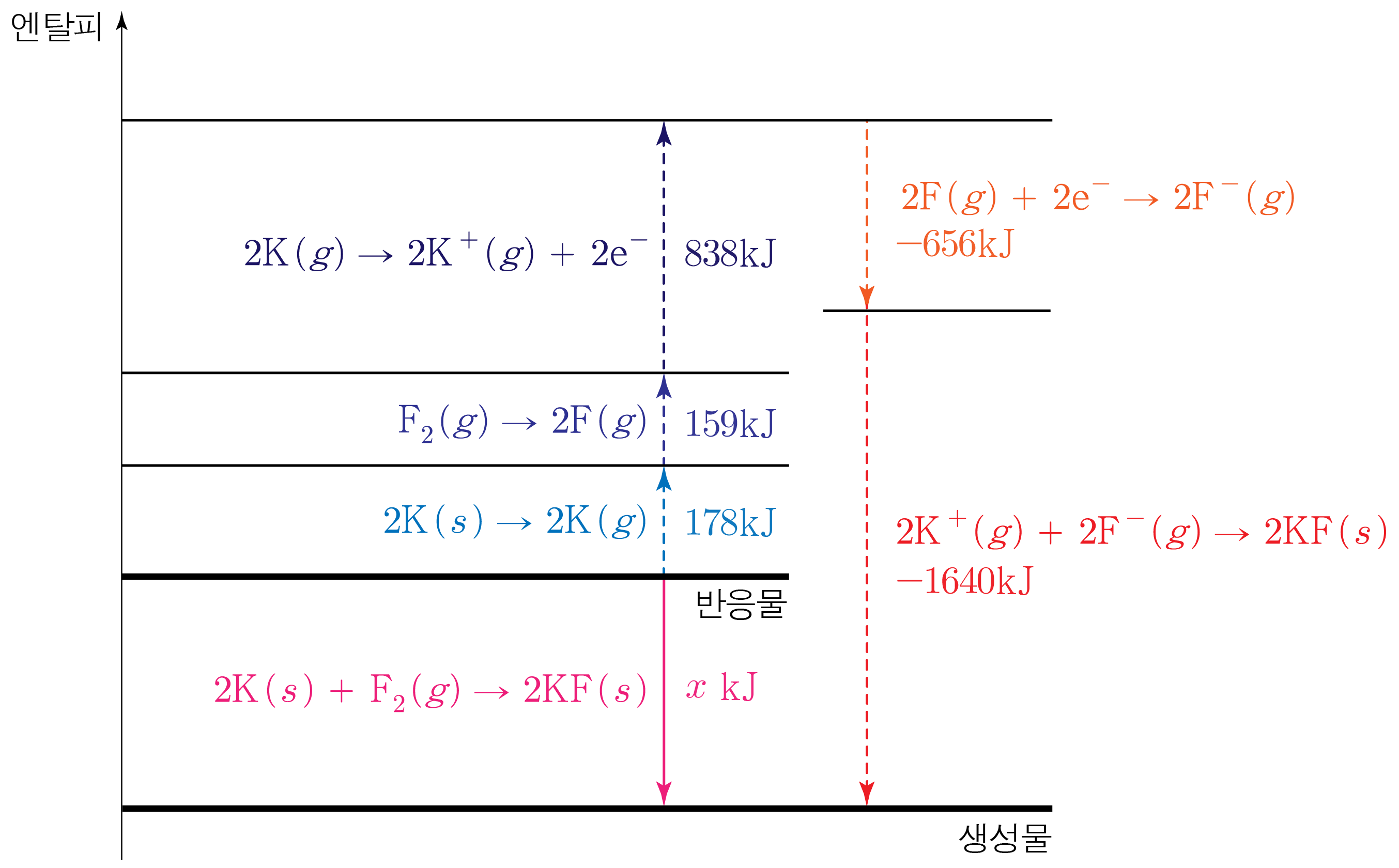
따라서 엔탈피 변화 과정을 나타내면 아래 그림과 같다.
그러므로
178kJ+159kJ+838kJ−656kJ−1640kJ=xkJ,
337kJ+838kJ−656kJ−1640kJ=xkJ,
1175kJ−656kJ−1640kJ=xkJ,
519kJ−1640kJ=xkJ,
−1121kJ=xkJ,
x=−1121이다.
따라서 답은 3번이다.
정답: $4$
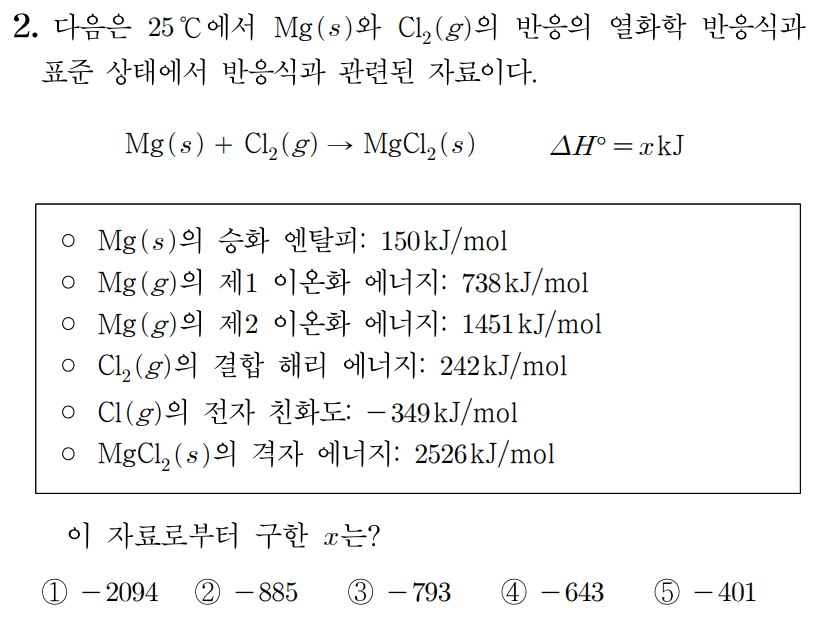
1. 반응물의 공유 결합을 모두 끊고 기체 상태의 중성 원자로 만든다. (결합 해리 에너지, 상변화 에너지 활용)
-
Cl2(g)의 결합 해리 에너지가 242kJ/mol이므로
Cl2(g) 1mol에서 Cl 원자 사이의 공유 결합을 모두 끊어 Cl(g) 2mol을 만들 때 흡수되는 에너지는
242kJ이다.
-
Mg(s)의 승화 엔탈피가 150kJ/mol이므로
Mg(s) 1mol을 Mg(g) 1mol로 만들 때 흡수되는 에너지는
150kJ/mol×1mol=150kJ이다.
2. 생성물에서 양이온을 이루는 원소의 중성 원자를 양이온으로 이온화시킨다. (이온화 에너지 활용)
생성물인 MgCl2(s)에서 양이온은 Mg2+에 해당하므로 양이온을 이루는 원소인 Mg를 양이온으로 이온화시킨다.
Mg(g)의 제1 이온화 에너지는 738kJ/mol이므로
Mg(g) 1mol에서 전자 1mol을 떼어 내어 Mg+(g) 1mol을 만들 때 흡수되는 에너지는
738kJ/mol×1mol=738kJ이다.
Mg(g)의 제2 이온화 에너지는 1451kJ/mol이므로
Mg+(g) 1mol에서 전자 1mol을 떼어 내어 Mg2+(g) 1mol을 만들 때 흡수되는 에너지는
1451kJ/mol×1mol=1451kJ이다.
3. 생성물에서 음이온을 이루는 원소의 중성 원자를 음이온으로 이온화시킨다. (전자 친화도 활용)
생성물인 MgCl2(s)에서 음이온은 Cl−에 해당하므로 음이온을 이루는 원소인 Cl을 음이온으로 이온화시킨다.
Cl(g)의 전자 친화도는 −349kJ/mol이므로
Cl(g) 2mol에서 전자 2mol을 추가하여 Cl−(g) 2mol을 만드는 데 방출되는 에너지는
349kJ/mol×2mol=698kJ이다.
4. 양이온과 음이온을 결합시켜 이온 결합 물질을 만든다. (격자 에너지 활용)
MgCl2(s)의 격자 에너지는 2526kJ/mol이므로
Mg2+(g) 1mol과 Cl−(g) 2mol이 반응하여 MgCl2(s) 1mol을 만들 때 방출되는 에너지는
2526kJ/mol×1mol=2526kJ이다.
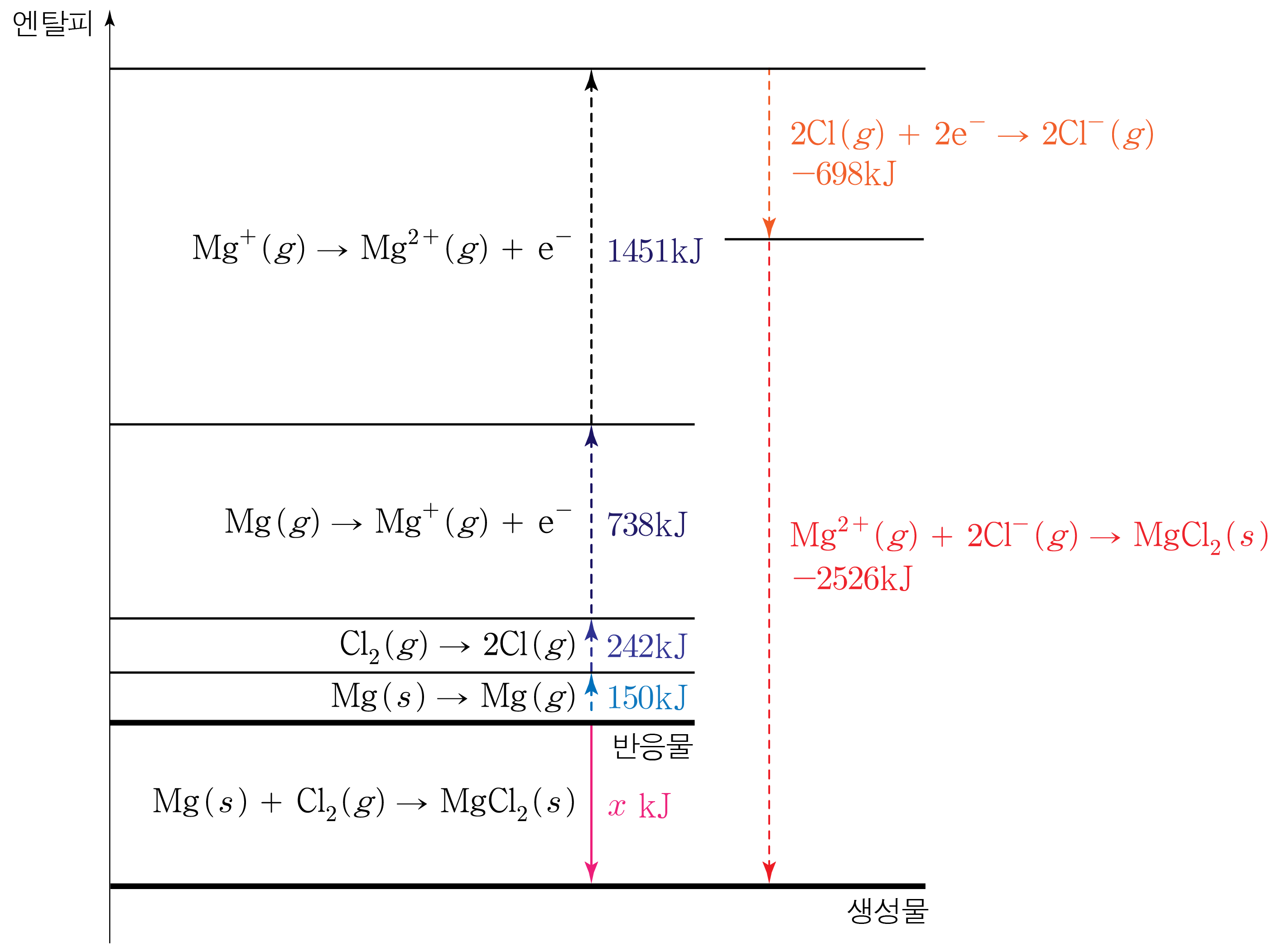
따라서 엔탈피 변화 과정을 나타내면 아래 그림과 같다.
그러므로 150kJ+242kJ+738kJ+1451kJ−698kJ−2526kJ=xkJ,
392kJ+738kJ+1451kJ−698kJ−2526kJ=xkJ,
1130kJ+1451kJ−698kJ−2526kJ=xkJ,
2581kJ−698kJ−2526kJ=xkJ,
1883kJ−2526kJ=xkJ,
−643kJ=xkJ,
x=−643kJ이다.
따라서 답은 4번이다.