| 해당 지식 |

|
| 하위 지식 |
상위 지식 |

|
$-$
|
정반응은 반응물이 생성물로 되는 반응이고, 역반응은 생성물이 반응물로 되는 반응이다.
가역 반응은 반응 조건(온도, 압력, 농도 등)에 따라 정반응과 역반응이 모두 일어날 수 있는 반응이고,
비가역 반응은 역반응이 거의 일어나지 않는 반응이다.
가역 반응의 화학 반응식에서는 화살표를 → 대신 ⇌를 사용한다.
물을 냉동실에 넣으면 얼음이 되지만 방 안에 놓으면 다시 녹아 물이 된다.
메테인(CH4)을 태우면 이산화탄소와 물이 생성되지만,
이산화탄소와 물로 다시 메테인과 산소를 생성하는 반응은 거의 일어나지 않는다.
CH4(g)+2O2(g)→CO2(g)+2H2O(l)
겉보기에는 반응이 일어나지 않는 것처럼 보이지만, 정반응과 역반응이 같은 속도로 일어나는 상태이다.
동적 평형 상태에서 평형을 이루는 두 물질의 질량은 일정하다.
동적 평형에서 2가지 이상의 상태가 공존할 때는 상평형이라고도 한다.
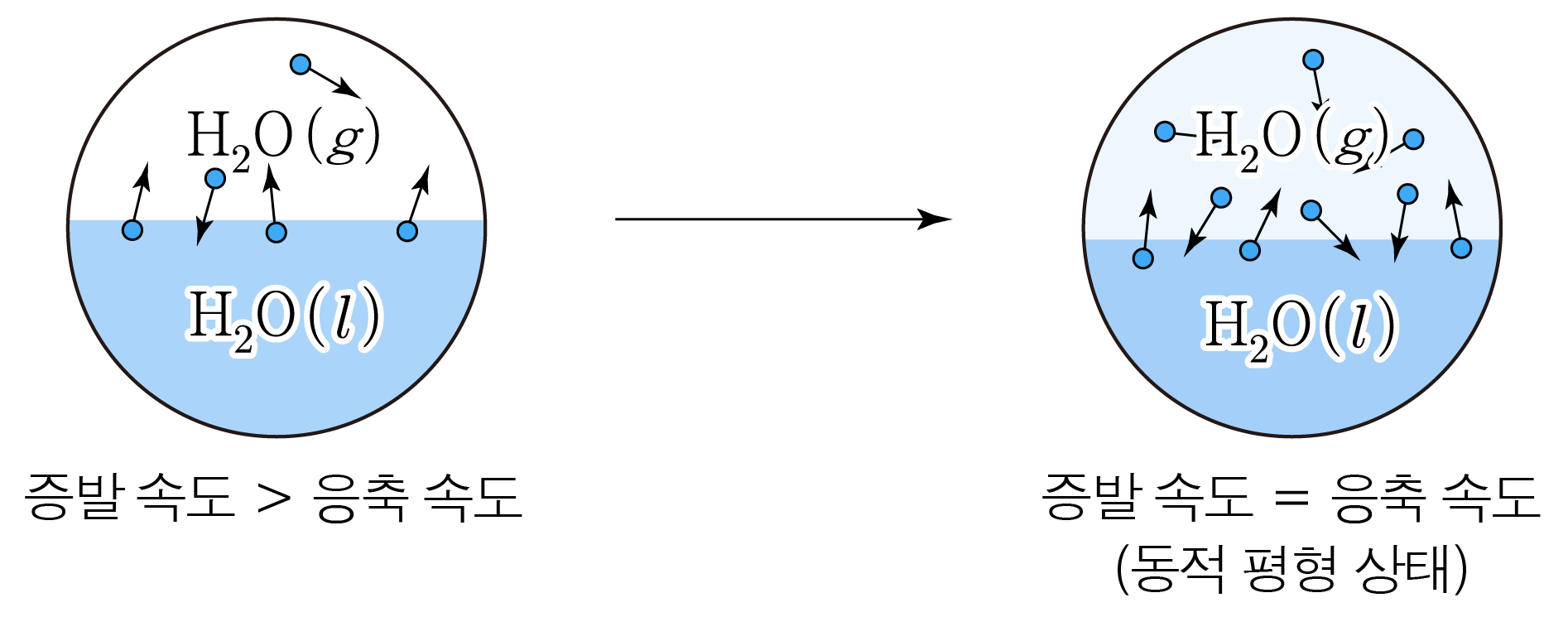
- 밀폐된 진공 용기 안에 충분한 양의 H2O(l)를 넣은 경우
초기에는 H2O(l)의 증발 속도가 응축 속도보다 크지만
시간이 지나면서 응축 속도가 점점 커져 증발 속도와 같아지는 동적 평형 상태에 도달한다.
H2O(l)⇌H2O(g)
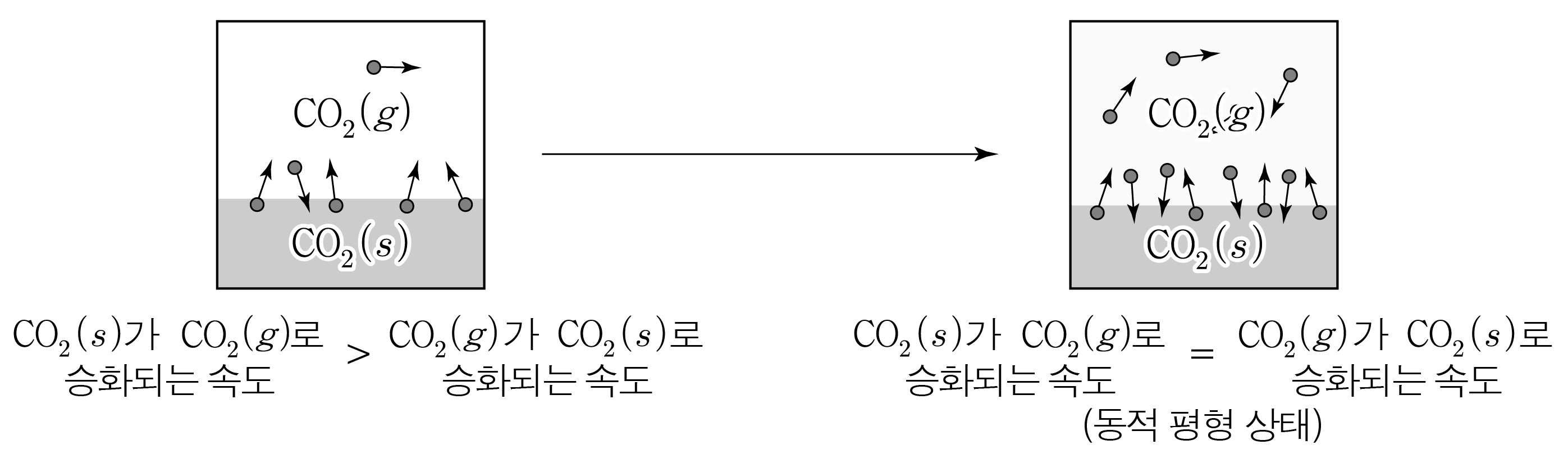
- 밀폐된 진공 용기 안에 충분한 양의 드라이아이스(CO2(s))를 넣은 경우
초기에는 CO2(s)가 CO2(g)로 승화되는 속도가 CO2(g)가 CO2(s)로 승화되는 속도보다 크지만
시간이 지나면서 CO2(g)가 CO2(s)로 승화되는 속도가 점점 커져 두 승화 속도와 같아지는 동적 평형 상태에 도달한다.
CO2(s)⇌CO2(g)
정답: $5$
ㄱ. 초기에는 증발 속도가 응축 속도보다 빠르므로 ㉠은 H2O(l)의 증발 속도이다. (O)
ㄴ. 동적 평형 상태에서는 정반응과 역반응이 같은 속도로 일어나므로 t2일 때 동적 평형 상태에 도달한다. (O)
ㄷ. 동적 평형 상태에서는 정반응과 역반응이 같은 속도로 일어나므로 평형을 이루는 두 물질의 질량은 일정하다.
그러므로 H2O(l)의 질량은 t3일 때와 t4일 때가 같다. (O)
따라서 답은 5번이다.
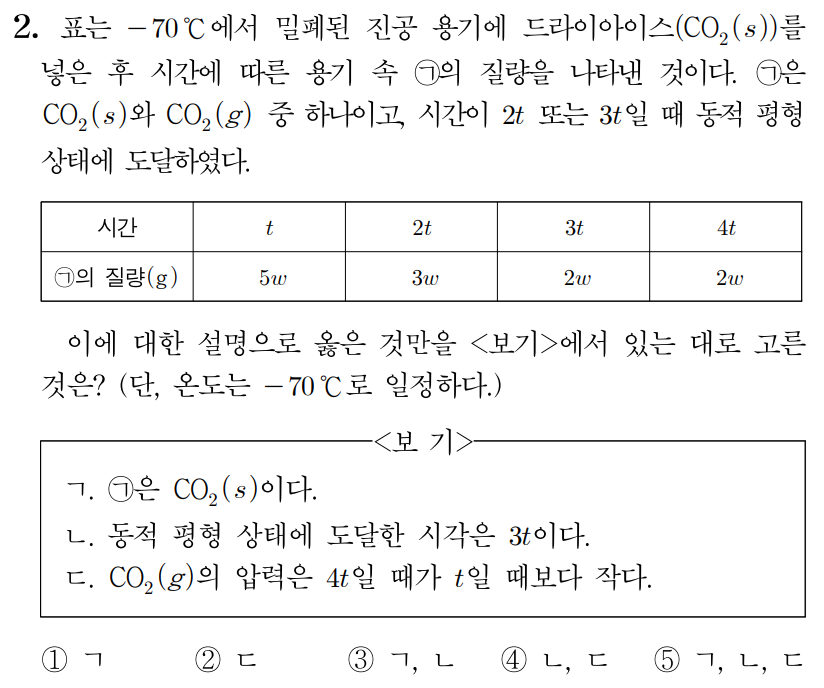
정답: $3$
ㄱ. 초기에는 CO2(s)가 CO2(g)로 승화하므로 CO2(s)의 질량은 감소하고 CO2(g)의 질량은 증가한다.
표에서 시간이 지날수록 ㉠은 감소하므로 ㉠은 CO2(s)임을 알 수 있다. (O)
ㄴ. 동적 평형 상태에서는 정반응과 역반응이 같은 속도로 일어나므로 평형을 이루는 두 물질의 질량은 일정하다.
그러므로 3t일 때 동적 평형 상태에 도달하였음을 알 수 있다. (O)
ㄷ. CO2(s)의 질량이 감소한 만큼 CO2(g)의 질량이 증가하므로 밀폐된 용기 내부 CO2(g)의 압력이 증가한다.
그러므로 CO2(g)의 압력은 4t일 때가 t일 때보다 크다. (X)
따라서 답은 3번이다.