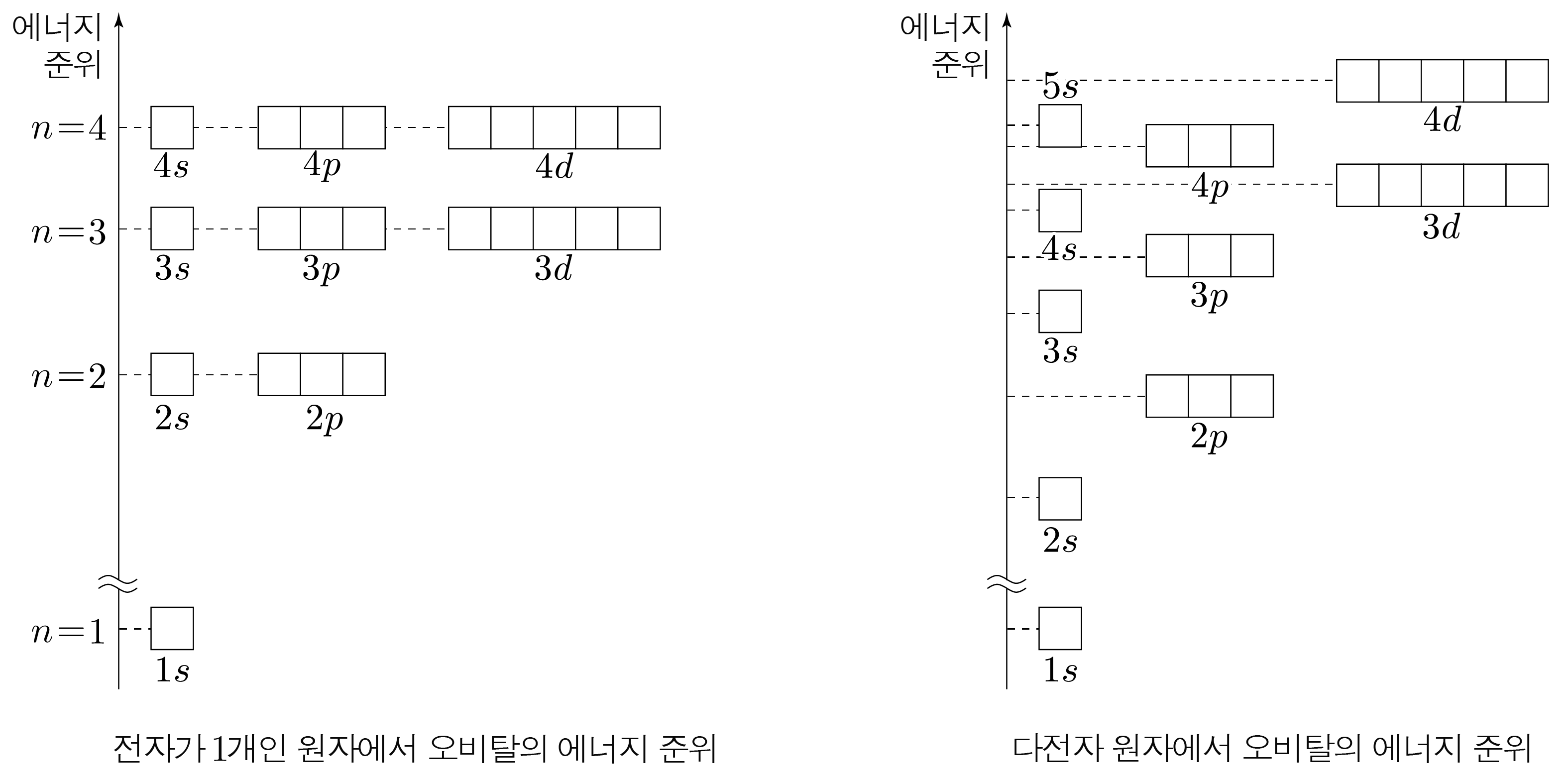
전자가 1개인 원자는 오비탈의 종류에 관계없이 주양자수에 의해서만 결정된다.
에너지 준위 비교: 1s<2s=2p<3s=3p=3d<⋯
전자가 2개 이상인 다전자 원자는 주양자수가 같더라도 오비탈의 종류에 따라 에너지 준위가 달라진다.
에너지 준위 비교: 1s<2s<2p<3s<3p<4s<3d⋯
3p<4s<3d임에 주의한다.
쌓음 원리, 파울리 배타 원리, 훈트 규칙을 따른다.
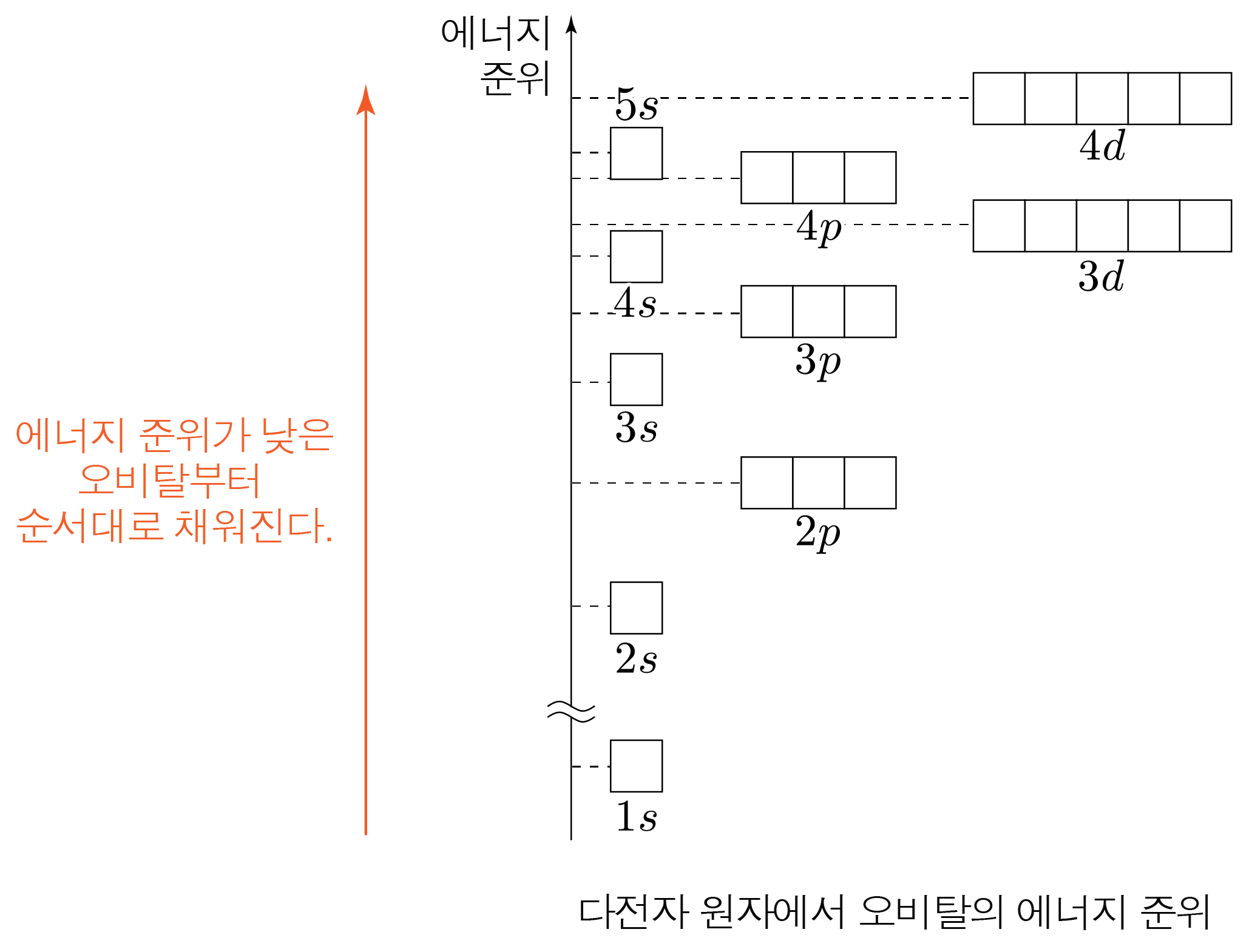
전자는 에너지 준위가 낮은 오비탈부터 순서대로 채워진다.
전자가 2개 이상인 다전자 원자의 에너지 준위는
1s<2s<2p<3s<3p<4s<3d⋯ 이므로
1s→2s→2p→3s→3p 순으로 전자가 채워지다가 3p에 모든 전자가 채워지면, 4s에 전자가 채워지기 시작한다.
칼슘(Ca)의 전자 배치 순서를 구해보자.
칼슘(Ca)은 원자 번호가 20이고, 중성 원자이므로 20개의 전자를 갖는다.
전자가 2개 이상인 다전자 원자의 에너지 준위는
1s<2s<2p<3s<3p<4s<3d⋯ 이므로
1s→2s→2p→3s→3p→4s 순으로 전자가 채워진다.
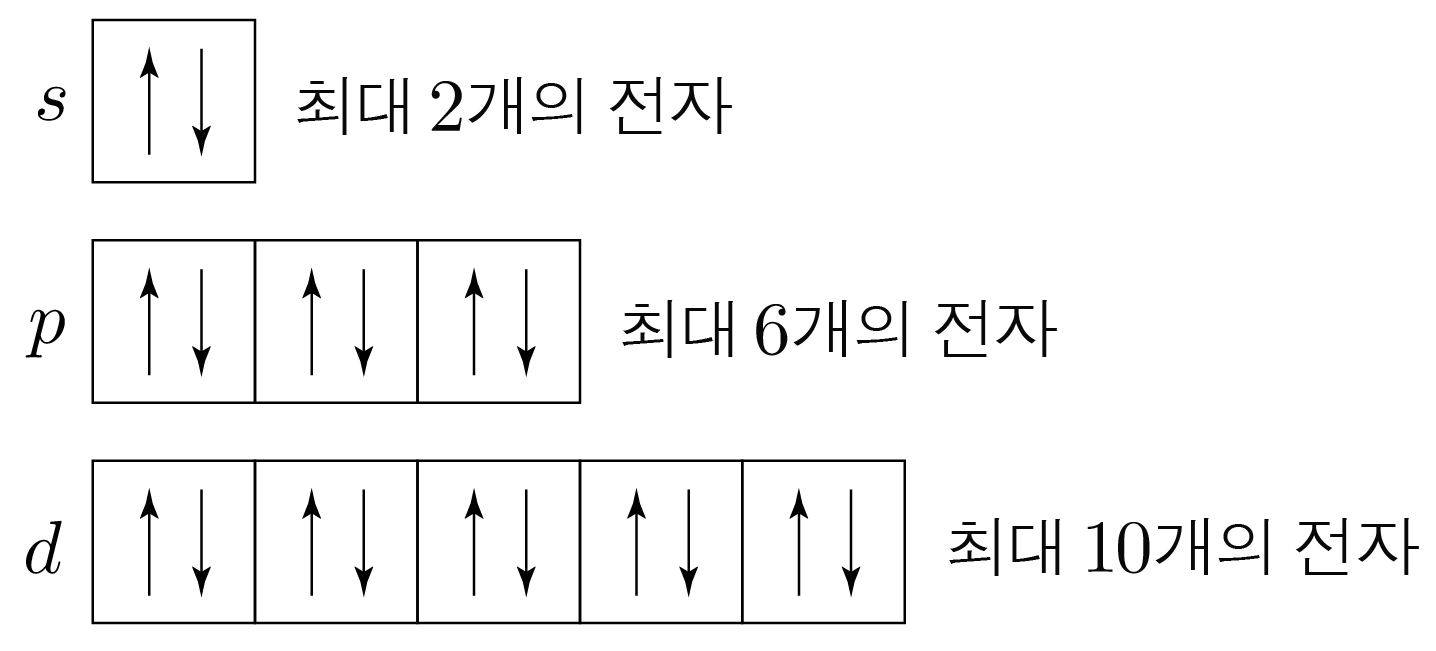
이때 s 오비탈에는 전자가 최대 2개, p 오비탈에는 전자가 최대 6개까지 채워지므로, 전자 배치는
1s(2개) → 2s(2개) → 2p(6개) → 3s(2개) → 3p(6개) → 4s(2개)와 같다.
1개의 오비탈에는 전자가 최대 2개까지 채워지며, 이 두 전자는 서로 다른 스핀 자기 양자수를 갖는다.
1개의 오비탈에는 전자가 최대 2개까지 채워지므로 3개 이상은 들어갈 수 없으며,
1개의 오비탈 내의 두 전자는 서로 다른 스핀 자기 양자수를 가지므로, 화살표의 방향은 서로 반대이다.
칼륨(K)의 전자 배치를 그려보자.
칼륨(K)은 원자 번호가 19이고, 중성 원자이므로 19개의 전자를 갖는다.
전자가 2개 이상인 다전자 원자의 에너지 준위는
1s<2s<2p<3s<3p<4s<3d⋯ 이므로
1s→2s→2p→3s→3p→4s 순으로 전자가 채워진다.
이때 s 오비탈에는 전자가 최대 2개, p 오비탈에는 전자가 최대 6개까지 채워지므로, 전자 배치는
1s(2개) → 2s(2개) → 2p(6개) → 3s(2개) → 3p(6개) → 4s(1개)와 같다.
따라서 전자 배치를 그림과 수식으로 나타내면 아래 그림과 같다.
- 그림으로 나타낼 때:
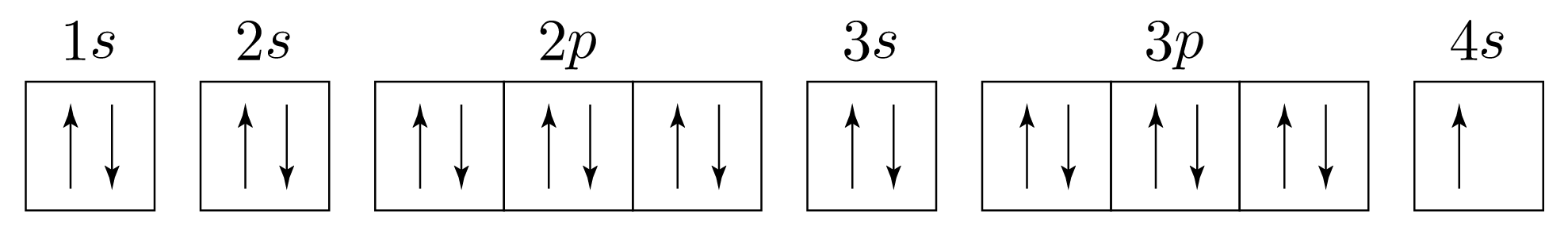
- 수식으로 나타낼 때: 1s22s22p63s23p64s1
에너지 준위가 같은 오비탈이 여러 개 있을 때, 전자는 쌍을 이루지 않는 전자(홀전자) 수가 최대가 되도록 배치된다.
탄소(C)의 전자 배치를 그려보자.
탄소(C)는 원자 번호가 6이고, 중성 원자이므로 6개의 전자를 갖는다.
전자가 2개 이상인 다전자 원자의 에너지 준위는
1s<2s<2p<3s<3p<4s<3d⋯ 이므로
1s→2s→2p 순으로 전자가 채워진다.
1s, 2s에 각각 전자가 2개씩 채워지고, 2p에 나머지 전자 2개가 채워질 때,
홀전자 수가 최대가 되도록 배치되므로 2p의 서로 다른 오비탈에 배치된다.
따라서 전자 배치를 그림과 수식으로 나타내면 아래 그림과 같다.
- 그림으로 나타낼 때:
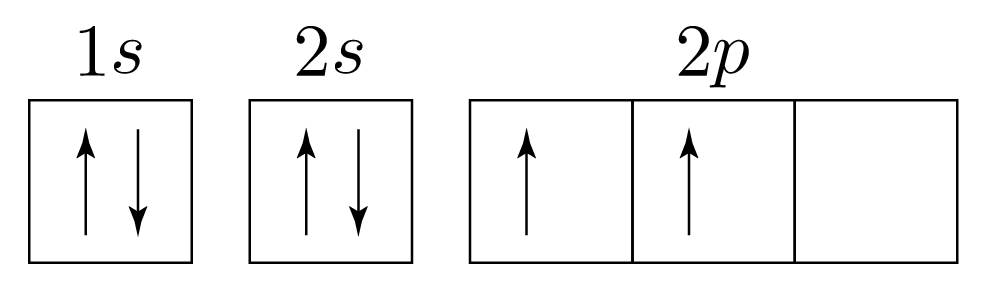
- 수식으로 나타낼 때: 1s22s22p2
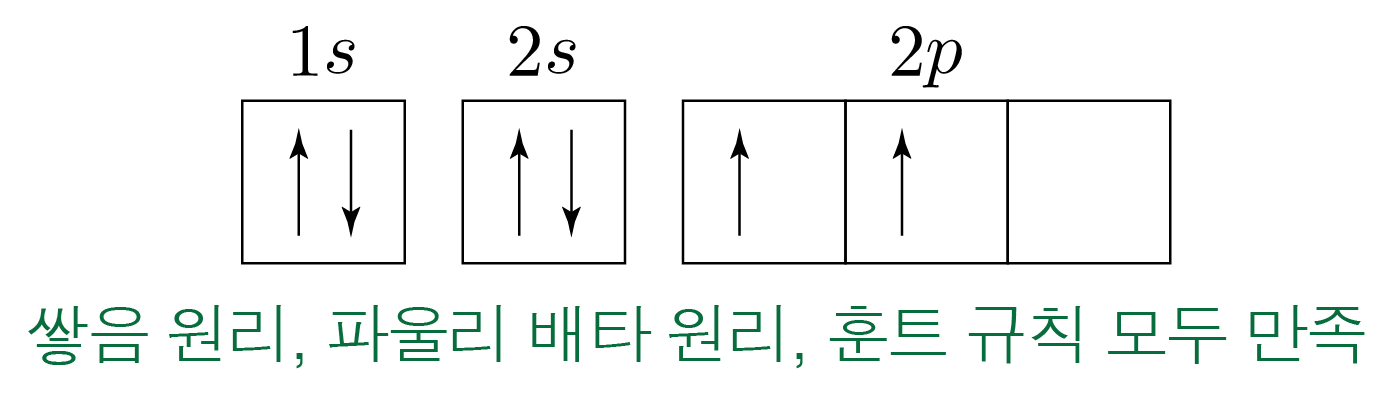
쌓음 원리, 파울리 배타 원리, 훈트 규칙을 모두 만족한 상태이다.
바닥 상태인 탄소 원자의 전자 배치를 나타내면 아래 그림과 같다.
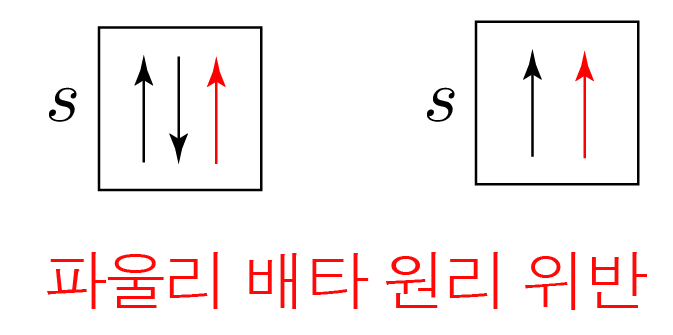
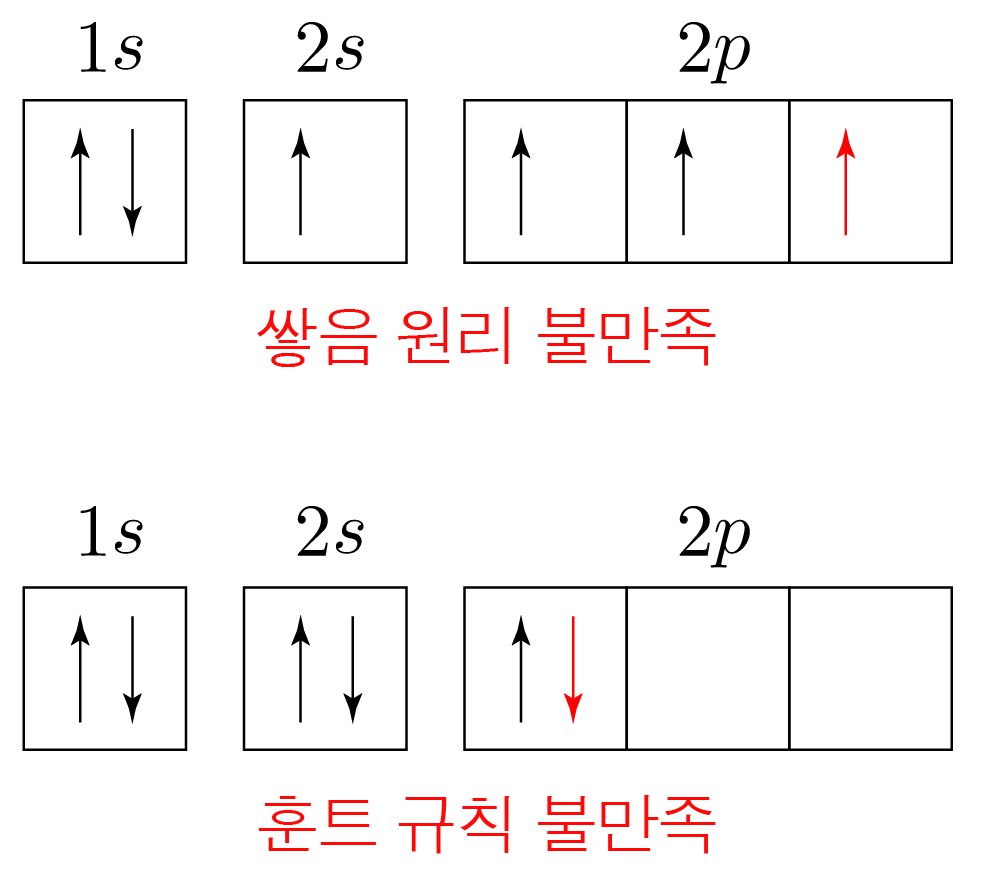
파울리 배타 원리는 만족하지만 쌓음 원리나 훈트 규칙을 만족하지 않는 상태이다.
탄소 원자의 들뜬 상태의 전자 배치 예시를 나타내면 아래 그림과 같다.
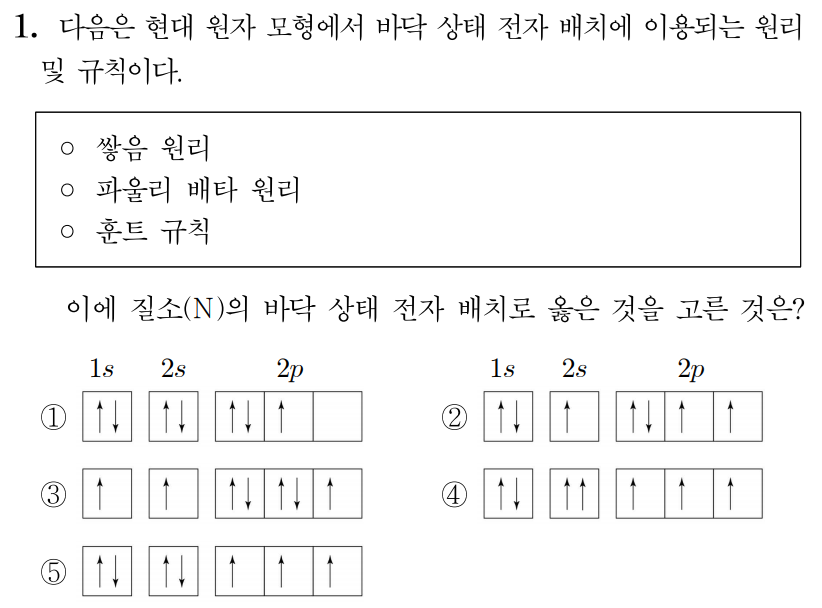
정답: $5$
질소(N)의 바닥 상태 전자 배치를 그려보자.
질소(N)는 원자 번호가 7이고, 중성 원자이므로 7개의 전자를 갖는다.
전자가 2개 이상인 다전자 원자의 에너지 준위는
1s<2s<2p<3s<3p<4s<3d⋯ 이므로
1s→2s→2p 순으로 전자가 채워진다.
1s, 2s에 각각 전자가 2개씩 채워지고, 2p에 나머지 전자 3개가 채워질 때,
홀전자 수가 최대가 되도록 배치되므로 2p의 서로 다른 오비탈에 배치된다.
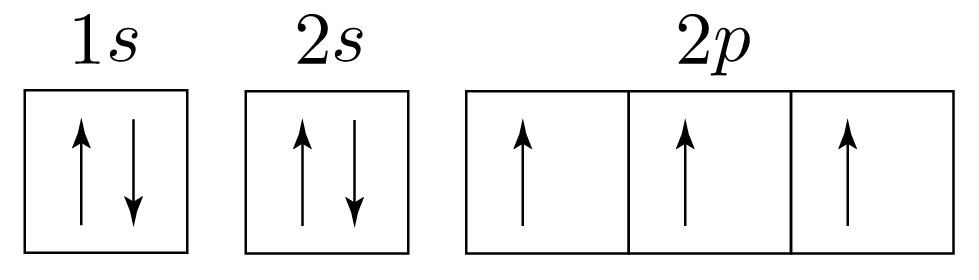
그러므로 전자 배치를 그림으로 나타내면 아래 그림과 같다.
4번은 2s의 전자가 서로 같은 방향이므로 파울리 배타 원리를 위반한다.
따라서 답은 5번이다.